В этой статье я объясню основное биологическое действие инсулина, Оно выходит далеко за рамки регуляции углеводного обмена и утилизации глюкозы, без этих сведений понять смысл процессов сахарного диабета, причины развития осложнений и правильно лечить сахарный диабет невозможно. Из-за разрозненности знаний, случайной или умышленной, эти сведения не попали в большинство учебников и монографий, посвященных сахарному диабете.
Когда нибудь я подготовлю более подробный, эмоциональный, обзор этих книг, которые помогали мне анализировать современное состояние сахарного диабета. Потому что они того стоят! Эти книги и мои учителя, встретились мне так вовремя, как настоящие друзья, и до сих пор я цитирую и цитирую именно их. Я это сообщаю здесь и сейчас лишь для того, чтобы сказать, что больше нигде такая информация мне уже не встречалась. За 20 лет поиска аргументов для гипотезы приспособительного значения сахарного диабета я не пропустила ни одного источника, не посмотрев, а как он определяет биологическое действие инсулина.
На тривиальный уже вопрос: «Для чего нужен инсулин?», — большинство врачей, ученых, статей т монографий по диабету, эндокринологии, физиологии, биохимии и других, незамедлительно отвечают: «Для регуляции уровня глюкозы!». Некоторые добавят: «Регуляции транспорта глюкозы в клетку!». Но самое удивительное, что, тиражируемая из статьи в статью, из монографии в монографию, мысль о регуляции инсулином избирательного транспорта глюкозы в клетку, не подтвердилась данными электронной микроскопии.
 Об этом написал Гильберт Линг в своей книге "Физическая теория живой клетки. Незамеченная революция".
Об этом написал Гильберт Линг в своей книге "Физическая теория живой клетки. Незамеченная революция".
Г. Линг подсчитал, что при использовании избирательных каналов для поддержания градиентов Na+ и K+ клетке потребовалось бы в 3600 раз больше энергии, чем она в действительности способна запасать.
 «Гормонотерапия» 1991 года под редакцией Шамбаха, недавно, после 18- летней разлуки, я снова держу её в руках и могу процитировать вам из нее (с. 185, последний абзац):
«Гормонотерапия» 1991 года под редакцией Шамбаха, недавно, после 18- летней разлуки, я снова держу её в руках и могу процитировать вам из нее (с. 185, последний абзац):
«Инсулин повышает проницаемость мышечных и жировых клеток для глюкозы, аминокислот, свободных жирных кислот, калия, магния и фосфатов.»
Что новенького?
В миофибриллозах, гепатоцитах и адипоцитах инсулин связывается с рецепторами на плазматической мембране и координирует анаболические реакции на доступность питательных веществ. При связывании инсулина с его рецептором активируется сигнальный каскад событий, в конечном счете способствующих поглощению глюкозы, особенно в мышечных и жировых тканях, которые экспрессируют высокие уровни транспортера GLUT4. Кроме того, действие инсулина влияет на усвоение жирных кислот, аминокислот и калия мышечными и жировыми тканями.
da Silva Rosa SC, Nayak N, Caymo AM, Gordon JW. Mechanisms of muscle insulin resistance and the cross-talk with liver and adipose tissue. Physiol Rep. 2020 Oct;8 (19):e14607. doi: 10.14814/phy2.14607. PMID: 33038072; PMCID: PMC7547588.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7547588/

Третья книга, как третий богатырь, — «Рецепторы» П.В. Сергеев и Н.Л. Шимановский, 1987. В ней я прочитала о кластерном расположении инсулиновых рецепторов, о формировании «корзинок» — заготовок пиноцитозных пузырьков, благодаря которым клетка делает «глоток», захватывая из околоклеточного пространства все, что там находится вместе с водой.
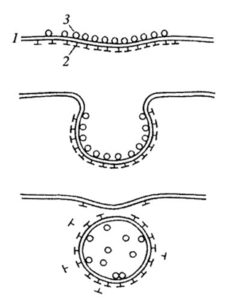 Рецепторы к инсулину образуют кластеры по 3-12 молекул в окаймленных ямках цитоплазматической мембраны. Эти ямки есть почти у всех клеток животных, занимая, как правило, около 2% клеточной поверхности. Их количество меняется в зависимости от потребности клетки, при ее снижении погружая этот участок в эндоплазматический ретикулум. Основное место работы инсулина — поверхностная мембрана. Он выполняет роль «привратника», замыкая корзинку в везикулу вместе со всем содержимым.
Рецепторы к инсулину образуют кластеры по 3-12 молекул в окаймленных ямках цитоплазматической мембраны. Эти ямки есть почти у всех клеток животных, занимая, как правило, около 2% клеточной поверхности. Их количество меняется в зависимости от потребности клетки, при ее снижении погружая этот участок в эндоплазматический ретикулум. Основное место работы инсулина — поверхностная мембрана. Он выполняет роль «привратника», замыкая корзинку в везикулу вместе со всем содержимым.
Рецепторы к инсулину обнаружены и внутри клетки на мембранах эндоплазматического ретикулума, комплекса Гольджи и ядер. Инсулиновых рецепторов ядерных мембран меньше, у них пониженное сродство к инсулину, чем у рецепторов плазматических мембран. Наряду с последними рецепторы ядерных мембран принимают участие в связывании гормона и в реализации его биологической активности. Поэтому поиски так называемых нарушений пострецепторного механизмов действия инсулина не увенчались успехом, но показали высокую экономичность и пластичность взаимодействия инсулина с тканями. Пострецепторным сигналом являются субстраты питания. Действие инсулина на клетки не требует синтеза вторичного посредника, некоторые метаболические эффекты инсулина могут реализовываться и без участия тирозинкиназного каскада, часто одна и та же молекулярная стратегия используется для достижения разных эффектов.
Важно заметить, что гомеостаз — это постоянство концентрации, что все вещества находятся в растворенном состоянии, окружены биполями воды.
Итак, благодаря инсулину внутрь клетки поступают все вещества, в том числе лекарственные препараты, другие гормоны, нуклеотиды и прочие.
Позднее выяснились и другие обстоятельства.
Уже древние бактерии использовали отходы жизнедеятельности для межклеточных коммуникаций. Впоследствии они стали выполнять функции гормонов. Например, при производстве человеческого инсулина и его аналогов генномодифицированные штаммы E.coli выделяют инсулин в питательную среду.
Не только инсулин, но и другие гормоны обнаружены у растений и животных разных уровней развития. Структура гормонов в процессе эволюции в основном не изменялась. Инсулин можно обнаружить у бактерий, одноклеточных, растений, кольчатых червей, моллюсков, насекомых и других организмов, не имеющих панкреатической железы, и у всех млекопитающих. Последовательность аминокислотных остатков в молекуле инсулина изучена у 25 и более видов животных. Установлено наличие инсулина и рецепторов к нему в неоплодотворенных куриных яйцах и эмбрионах цыплят 2-3 дневного возраста, в плаценте, эмбрионах и желточном мешке крысы, слюнных железах. В эмбриогенезе многоклеточных ряд гормонов выявляется в первые часы и дни развития.
Обеспечение питания β-клеток зависит от инсулина в той же мере, как и любых других клеток организма, β-клетки поджелудочной железы имеют на своей клеточной мембране рецепторы к инсулину. Только что выделенный инсулин взаимодействует со своим рецептором на мембране, возможно, его же секретировавшей β-клетки. Пополняя β-клетку необходимыми субстратами, инсулин инициирует синтез веществ, обеспечивающих ее функцию.
На протяжении многих лет головной мозг рассматривался как инсулино-независимый орган, способный утилизировать глюкозу без участия инсулина, однако эта точка зрения радикально пересмотрена,
Многими авторами признано, что инсулин транспортируется в физиологических условиях через гематоэнцефалический барьер. Транспорт инсулина в мозг затруднен при нейродегенерации, старении, голодании, ожирении, однако при некоторых формах СД и в периоде неонатального развития скорость транспорта инсулина в головной мозг увеличивается. Присутствие инсулина в культуре шванновских клеток обеспечивает ее поддержание и увеличение уровня пролиферации клеток при регенерации периферических нервов. Действие инсулина в клетках головного мозга протекает по тем же механизмам, что и в периферических тканях.
Доказано наличие инсулина в эритроцитах.
Важно понять, что инсулиннезависимых тканей не существует, поскольку рецепторы к инсулину обнаруживаются практически во всех клетках организма, их строение и связывающие свойства не зависят от типа ткани и вида животного.
В монографии «Физиология сахарного диабета» я собирала разнообразные факты эффектов инсулина в организме.
- Инсулин обеспечивает потребности клеточного гомеостаза, стимулирует синтез, тормозит распад, активирует геном, регулирует экспрессию ранних генов с-fos и с-jun;
- может выполнять антиоксидантные функции в организме, in vivo и in vitro вызывает торможение перекисного окисления липидов, проявляет антилиполитический и антиоксидантный эффекты, которые имеют возрастные и дозозависимые различия.
- Инсулин потенцирует свойства возбудимых тканей,
- регулирует процессы свертывания крови, обнаружена прямая корреляция между содержанием в крови инсулина и фибриногена, обратная зависимость с содержанием активатора плазминогена.
- Инсулин участвует в регуляции водно-солевого обмена: регуляции секреции альдостерона , обнаружена инсулинзависимость осморецепторов; стимулирует транспорт натрия в проксимальных и дистальных канальцах почек, активируя Na-К-АТФазу, повышает содержание натрия и мочевины в интерстициальной ткани мозгового вещества и почечном сосочке, задерживает натрий в организме, усиливая реабсорбцию, блокируя его экскрецию почками; модулирует центральную регуляцию артериального давления; является вазоактивным пептидом, вызывая дилатацию сосудов скелетной мускулатуры, ослабляя вазоконстрикцию через альфа-2-адренергический путь.
- Инсулин активирует гуморальные и клеточные иммунные реакции и гемопоэз, регулирует органогенез и дифференцировку у плода, участвует в регуляции функции яичника. РИ и ИФР-1 обнаружены в яичниках животных и человека,где оба вещества оказывают митогенный эффект, стимулируя пролиферацию клеток гранулезы в яичниках коров и свиней (но не мышей) in vitro; усиливают стероидогенез в яичниках, потенцируя эффект гонадотропинов; стимулируют синтез эстрадиола и прогестерона, индуцированный ФСГ, в клетках гранулезы и ЛГ-индуцированный синтез андростендиона в клетках теки и стромы, эти эффекты зависимы от дозы и времени. При совместном введении эти вещества не усиливают действие друг друга. Отмечено
прямое индуцирующее и активирующее влияние инсулина и ИФР-1 на ароматазу. Выявлено усиление ФСГ-зависимой выработки ЛГ-рецепторов в клетках гранулезы на фоне действия инсулина и ИПФР-1. - Инсулин, способствует восприятию мозгом информации о состоянии углеводного обмена и уровня массы тела, влияет на организацию процессов внимания, памяти, моторной активности, ориентировочно-исследовательских реакций, питьевого и пищевого поведения, обучения, социального поведения, коммуникабельности, агрессивности, болезненного пристрастия, регулирует пищевую мотивацию и насыщение. Показано повышение болевых порогов у здоровых животных при введении инсулина в желудочки мозга.
Эффекты инсулина многообразны, поскольку ни одна функция клеток, тканей и организма не происходит без субстратно-энергетического обеспечения, а значит и без инсулина
Анаболическое влияние инсулина указывает на его необходимость для осуществления функционирования всех тканей, органов и физиологических систем, реализации эмоциональных и поведенческих актов, поддержания гомеостаза, осуществления механизмов приспособления и защиты от неблагоприятных факторов среды.
Чувствительность к инсулину определяется числом рецепторов. Численность, качество рецепторов, их способность образовывать кластеры зависят от типа ткани, степени дифференцировки клеток, стратегии саморегуляции организма.
| Локализация рецепторов | Число участков на клетку |
| Гепатоциты | 50 000 |
| Адипоциты | 50 000 |
| — через 24 часа после удаления инсулина | 1-2 000 000 |
| Моноциты | 16 000 |
| Эритроцит | 40 |
| Синаптосомы мозга | 80 пмоль/1 мг белка |
| Эмбриональная карцинома | 11 200 |
| Клетки панкреатических островков | 0,58´ 10-17 моль/островок |
| Мембраны плаценты | 2,93-3,7 пмоль/1 мг белка |
| Асцитные клетки Эрлиха | 180 000 |
(Сергеев П.В., Шимановский Н.Л., 1987 )
Для максимального биологического эффекта инсулина в большинстве инсулинзависимых тканей достаточно занятости его молекулами только 5-10% клеточных рецепторов [Микаелян Н.П., Князев Ю.А.,1999].
Обнаружено повышение количества инсулиновых рецепторов при стрессе, ожоговой болезни, беременности, голоде [Микаелян Н.П.1988].
 Высокой чувствительностью к инсулину обладают молодые клетки. Рецепторы к инсулину у новорожденных крыс имеют большее сродство к гормону, они обнаруживаются в больших количествах, обладают низкой способностью к десенситизации. Скорость деградации инсулина у новорожденных крыс в 3 раза ниже, чем у взрослых.
Высокой чувствительностью к инсулину обладают молодые клетки. Рецепторы к инсулину у новорожденных крыс имеют большее сродство к гормону, они обнаруживаются в больших количествах, обладают низкой способностью к десенситизации. Скорость деградации инсулина у новорожденных крыс в 3 раза ниже, чем у взрослых.
Гиперинсулинемия более губительно влияет на молодых (летальность 46,7 %), чем на старых особей (летальность 10 %) [Poljak-Blazi M. et al. ,1992, Сергеев П.В., Шимановский Н.Л.,1987].
 Куда направится инсулин? Туда где выше чувствительность. Туда, где выше активность.
Куда направится инсулин? Туда где выше чувствительность. Туда, где выше активность.
Туда где лучше кровоток. Молодые, активные и прожорливые клетки первыми примут на себя вал секреции инсулина, стимулированного простыми углеводами и веществами, повреждающими поджелудочную железу.
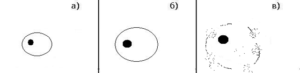 Некроз — это патологическая, форма клеточной гибели, в результате которой клетка набухает, увеличивается в размерах и разрушается
Некроз — это патологическая, форма клеточной гибели, в результате которой клетка набухает, увеличивается в размерах и разрушается
Некроз клетки. а) исходный вид клетки; б) небольшое набухание клетки; в) сильное набухание клетки, приводящее к разрыву мембраны
А как защитить организм от избыточного действия инсулина? Также как от избыточной еды.


Ранее показано [Lopez S., Desbuquois B.,1983], что введение крысам глюкозы (300 мг) вызывает пятикратное увеличение уровня инсулина в плазме и последующее уменьшение его связывания с поверхностными мембранами клеток печени на 20-25 %, но повышение его связывания с внутриклеточными мембранами комплекса Гольджи на 50-70 %. Повышение концентрации инсулина в крови приводит к быстрому и обратимому перемещению инсулиновых рецепторов с поверхности клетки внутрь гепатоцитов без изменения их общего числа.
Среди клеточных процессов, контролируемых инсулином, — транспортировка везикул, активность метаболических ферментов, факторы транскрипции и деградация самого инсулина. Saltiel AR. Insulin signaling in health and disease. J Clin Invest. 2021 Jan 4;131 (1):e142241. doi: 10.1172/JCI142241. PMID: 33393497; PMCID: PMC7773347. https://pubmed.ncbi.nlm.nih.gov/33393497/





