Вопрос «Куда устремляются питательные вещества под действием инсулина?» считаю чрезвычайно важным. я уже писала о том, что особенно уязвимы клетки мозга и почек, о том, что актуально это и для клеток постоянно обновляющихся — клеток стенки сосудов, эпителия, поэтому интенсивно происходит захват жировыми клетками и раковыми клетками. Что же потом происходит с клеткой? Она набухает, пытается этот наплыв перераспределить, это называется эндоплазматическим стрессом. Потому что это структура представляет собой вроде «пулеметной ленты» погружаемой с поверхности клеток внутрь мембрану, которая переносит пиноцитозные везикулы. Как я уже писала в статье «Биологическое действие инсулина», пиноцитоз регулируется именно им и никаким другим гормоном.
Вопрос «Куда устремляются питательные вещества под действием инсулина?» считаю чрезвычайно важным. я уже писала о том, что особенно уязвимы клетки мозга и почек, о том, что актуально это и для клеток постоянно обновляющихся — клеток стенки сосудов, эпителия, поэтому интенсивно происходит захват жировыми клетками и раковыми клетками. Что же потом происходит с клеткой? Она набухает, пытается этот наплыв перераспределить, это называется эндоплазматическим стрессом. Потому что это структура представляет собой вроде «пулеметной ленты» погружаемой с поверхности клеток внутрь мембрану, которая переносит пиноцитозные везикулы. Как я уже писала в статье «Биологическое действие инсулина», пиноцитоз регулируется именно им и никаким другим гормоном.
Актуальность
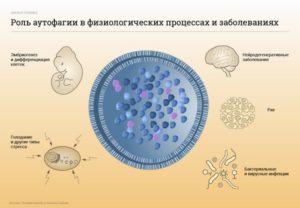
Значение аутофагии (буквально — самопожирание) при сахарном диабете является насущной проблемой, в последнее время широко обсуждается в научной периодике. При сахарном диабете организму не хватает прежде всего белков.Аутофагия является основным внутриклеточным процессом, который влияет на физиологию человека не только при сахарном диабете, но и в широком спектре состояний и заболеваний.
Суть процесса
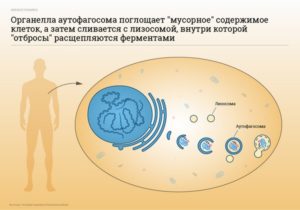
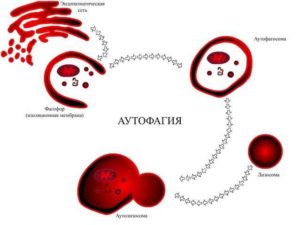
Аутофагия — это катаболический гомеостатический процесс, который заключается в необходимости разлагать и перерабатывать внутриклеточные белки и поврежденные органеллы, контролируя сохранение нормальных клеточных функций. Аутофагия является основным внутриклеточным путем деградации, разделения некоторых цитоплазматических компонентов, в том числе накопленных белков, поврежденных органелл, или вторгающихся микроорганизмов, которые выделяются в отдельную везикулу и доставляются в лизосомы для деградации.
Биологическое значение
- Аутофагия является основным катаболическим механизмом деградации дисфункциональных белков, а также дефектных клеточных компонентов. Во время развития СД2 аутофагия усиливается.
- Аутофагия представляет собой эволюционно консервативные механизм, с помощью которого цитоплазматические элементы разрушаются внутри клеток. Это можно сравнить с помещением ненужных файлов в корзину, или почтовых сообщений в папку спам
- Аутофагия защищает клетки от воздействия различных стресс-факторов.
- Аутофагия действует как обоюдоострый меч при мягком стрессе и помогает клетке выживать во время сильного стресса.
- Нарушение аутофагии приводит к массовой смерти клеток и может играть роль в инициации обострения.
- Аутофагия является клеточным контролем качества, тесно взаимосвязанным с иммунитетом. Связь между этими аспектами являются ключом ко многим заболеваниям человека, в том числе нейродегенерации, ожирению и диабету, хроническим воспалительным заболеваниям, раку, инфекциям и старению.
- Аутофагия участвует в апоптозе — программируемой клеточной смерти.
- Аутофагия регулирует переработку питательных веществ, производство энергии и органелл.
- Когда организму не хватает питания, благодаря аутофагии он использует белки своих собственных клеток. Аминокислоты белков — главное, чего не хватает организму при сахарном диаете
Клиническое значение при сахарном диабете
- Обнаружена усиленная аутофагия в клетках мышц, печени и жировых при сахарном диабете.
- Высокий уровень глюкозы напрямую ингибирует аутофагию. Полагаю, это полезная приспособительная реакция, чтобы защитить от апоптоза эндотелиальные клетки сосудов микроциркуляторного русла сердечной мышцы.
- Торможение аутофагии участвует в развитии диабета и индуцированных старением нарушениях сердечной деятельности.
- Аутофагия защищает панкреатические бета-клетки и их функции в условиях диеты с высоким содержанием жиров и глюкозы.
- Осложнения диабета сопровождаются чрезмерной активации аутофагии и увеличением апоптоза.
- Стресс эндоплазматического ретикулума (ЭР) и аутофагия модулируют выживание нейронов и связаны при поражениях мозга и нервной системы.
- Нарушения аутофагии имеет значение в развитии нефропатии и может способствовать как гломерулярным и тубуло интерстициальным заболеваниям почек при диабете.
- Аутофагии увеличиваются в клетках сетчатки у больных сахарным диабетом.
- Нарушение процессов аутофагии способствуют развитию сердечной кардиомиопатии. Аутофагия выступает в качестве основного регулятора сердечного гомеостаза и функции. Аутофагия сохраняет структуру и функцию сердца при исходных условиях и активизируется во время стресса, ограничивая повреждения в большинстве условий. Это уменьшает повреждения и сохраняет функцию сердца при ишемии. Происходит снижение полушарного ишемического ремоделирования, кроме того аутофагия способствует сердечной адаптации к давлению перегрузки, ограничивая накопление неправильно свернутых белков, митохондриальную дисфункцию и оксидативный стресс. Однако, массивная активация аутофагии может быть вредным для сердца при определенных стрессовых условиях, таких как реперфузии.
- Дефицит аутофагии гасит дифференциацию адипоцитов, тормозит развитие жировой ткани.
Торможение аутофагии происходит при старении клеток в условиях дефицита питания.
Физические упражнения стимулируют неселективную аутофагию и селективную аутофагию митохондрий в скелетных мышцах как у экспериментальных животных, так и у людей.
Хочу отметить, что без решения вопроса питательного обеспечения организма прежде всего белком проблему аутофагии при сахарном диабете не решить. Белка прежде всего не хватает организму при сахарном диабете.
Источники питательного белка
Что нужно есть при сахарном диабете?
10 и более проблем больных сахарным диабетом, которые решает белковое питание
Одни исследователи ратуют за стимуляцию аутофагии, другие за её предупреждение.
Одно ясно, аутофагия есть.
Что новенького?
В ответ на энергетические и метаболические потребности в периоды клеточного стресса клетки подвергаются более частой аутофагии и индуцируют катаболические процессы (Feng et al., 2014; He & Klionsky, 2009; Kroemer et al., 2010; Mizushima, 2018; Mizushima & Levine, 2010).
Этот механизм самоусвоения необходим для удаления поврежденных органелл и белков лизосомой. Происходит образование аутофагосомы, которая инкапсулирует груз для последующего разложения лизосомами (Badadani, 2012; Kroemer et al., 2010; Yang & Klionsky, 2010).
Первоначально предполагалось, что аутофагия является клеточным ответом на голодание или недостаток питательных веществ; однако некоторые исследования показали, что аутофагия потенциально может играть роль в предотвращении резистентности к инсулину в сытом состоянии. И наоборот, в других исследованиях утверждается, что аутофагия фактически способствует патогенезу резистентности к инсулину (Rocha et al., 2020).
Начало острой физической нагрузки может способствовать нарушению связи между комплексом Bc1-2‐Беклин‐1, что, следовательно, приводит к усилению аутофагии в скелетных мышцах.
У здоровых бегунов, тренированных на выносливость, ключевые маркеры митофагии, такие как PINK1 и Drp1, были повышены в скелетных мышцах, и пища с высоким содержанием жира не влияла на эти маркеры (Tarpey et al., 2017).
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7547588/
Другая недавняя работа продемонстрировала связь между физическими упражнениями и аутофагией в мышцах и показала, что физические упражнения очень эффективны в стимулировании аутофагии в скелетных мышцах, и что сопутствующий вывод поврежденных клеточных компонентов и дисфункциональных митохондрий имеет решающее значение для мышечного гомеостаза. Аутофагия — это катаболический процесс, который обеспечивает деградацию измененных / поврежденных органелл путем слияния аутофагосом и лизосом. Правильная регуляция аутофагического потока имеет фундаментальное значение для гомеостаза скелетных мышц в физиологических условиях и в ответ на стресс. Как недостаточная, так и чрезмерная аутофагия вредна для здоровья мышц и играет патогенную роль в нескольких формах мышечных заболеваний. Дефектная активация аутофагического механизма играет ключевую роль в патогенезе мышечных дистрофий, связанных с коллагеном VI. Нарушение аутофагического потока вызывает накопление дисфункциональных митохондрий и измененного саркоплазматического ретикулума, что приводит к апоптозу и дегенерации мышечных волокон. Примечательно, что физические тренировки усугубили дистрофический фенотип мышей Col6a1–/ –, у которых нарушен поток аутофагии. Аутофагия не индуцировалась в Col6a1–/– мышцах ни после острой, ни после длительной физической нагрузки, и это приводило к заметному увеличению мышечного истощения и апоптоза. Эти результаты показывают, что правильная активация аутофагии важна для мышечного гомеостаза во время физической активности. https://pubmed.ncbi.nlm.nih.gov/22024752/